نقش طراحی مبتنی بر کیفیت (QbD) در توسعه محصولات دارویی
20 اسفند 1402
ارسال شده توسط sasan_tonfa_admin
نقش طراحی مبتنی بر کیفیت (QbD) در توسعه محصولات دارویی
Quality by Design: مسیر علمی بهسوی محصول پایدار و قابل اعتماد
در دنیای امروز، صنعت داروسازی با الزامات رگولاتوری سختگیرانهتری نسبت به گذشته مواجه است. در این فضا، رویکردهای سنتی که تمرکز آنها بر آزمون کیفیت محصول نهایی است، دیگر پاسخگوی چالشهای پیچیده کیفیت، ریسک و پایداری نیستند. به همین دلیل، طراحی مبتنی بر کیفیت (QbD) بهعنوان یک رویکرد علمی، ساختاریافته و پیشگیرانه معرفی شده که بر درک عمیق فرآیند و محصول در طول چرخه عمر تأکید دارد.
مفهوم QbD چیست؟
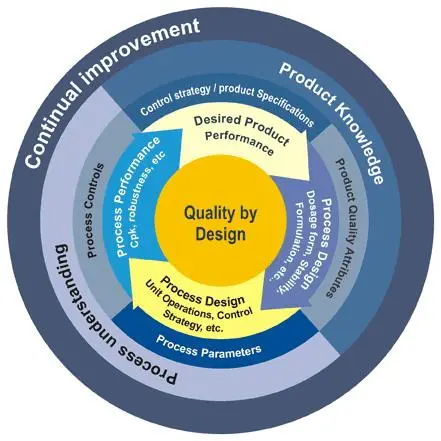
Quality by Design (QbD) مفهومی است که توسط ICH در راهنمای Q8 معرفی شده و بهمعنای «طراحی کیفیت از ابتدا» است. در این رویکرد، کیفیت محصول در مرحله طراحی و توسعه آن لحاظ شده و نه صرفاً در انتهای خط تولید با آزمون نهایی.
اجزای کلیدی QbD
1.پروفایل هدف محصول (QTPP)
مشخصات مورد انتظار از محصول نهایی شامل مسیر مصرف، دوز، شکل دارویی و عملکرد درمانی.
2.ویژگیهای کیفی بحرانی (CQAs)
ویژگیهایی از محصول که بر ایمنی و اثربخشی آن تأثیر مستقیم دارند (مانند اندازه ذرات، نرخ آزادسازی، پایداری).
3.ارزیابی ریسک
شناسایی متغیرهای بحرانی فرآیند (CPPs) و تأثیر آنها بر CQAs با ابزارهایی مانند FMEA.
4.Design Space
فضای عملیاتی مشخصی که تغییرات درون آن، بر کیفیت نهایی اثر منفی ندارد.
5.استراتژی کنترل (Control Strategy)
تعیین نقاط کنترل کلیدی و روشهای پایش، برای اطمینان از کیفیت مداوم در تولید.
مزایای QbD
•کاهش نیاز به تغییرات پس از تأیید (Post-approval changes)
•کاهش ریسک ریجکت و اصلاحات
•بهبود قابلیت اطمینان و پایداری در تولید
•تسهیل صدور مجوزهای بینالمللی (EMA/FDA)
•افزایش دانش فرآیند برای توسعه محصولات آینده
الزامات رگولاتوری
•ICH Q8(R2): توسعه دارویی بر اساس QbD
•ICH Q9: مدیریت ریسک کیفیت
•ICH Q10: سیستم مدیریت کیفیت دارویی
•ICH Q12: مدیریت چرخه عمر محصول دارویی
مثالهای کاربردی از QbD
•استفاده از طراحی آزمایشها (DOE) برای تعیین تأثیر نسبت اجزای فرمولاسیون بر نرخ آزادسازی
•طراحی سیستم پایش فرآیند (PAT) برای تولید محصولات تزریقی استریل
•توسعه روش HPLC مبتنی بر QbD برای تجزیه ناخالصیها
خدمات AVISAN در پیادهسازی QbD
شرکت AVISAN با تیمی متخصص و بینالمللی، آماده ارائه خدمات زیر در حوزه QbD است:
🔹 طراحی فرمولاسیون علمی با استفاده از QTPP و CQAs
🔹 توسعه روشهای تحلیلی پایدار و معتبر
🔹 ارزیابی ریسک و تدوین Design Space
🔹 اجرای DOE و تحلیل آماری نتایج
🔹 آموزش تیم توسعه محصول و تضمین کیفیت
🔹 مستندسازی کامل برای پروندههای CTD و ماژول 3
نتیجهگیری
در مسیر توسعه محصولات باکیفیت و پایدار، QbD دیگر یک انتخاب نیست؛ بلکه یک الزام است. با بهرهگیری از این رویکرد، نهتنها محصولی قابل اعتماد تولید میشود، بلکه فرایند توسعه، تولید و اخذ مجوز نیز علمی، سریع و مقرونبهصرفه خواهد بود
2 دیدگاه
به گفتگوی ما بپیوندید و دیدگاه خود را با ما در میان بگذارید.



این یک دیددگاه آزمایشی است.
تست پاسخ دیدگاه برای شما اینطور است.