مفهوم سیستم کیفی دارویی در خطوط راهنماها
20 اسفند 1402
ارسال شده توسط sasan_tonfa_admin
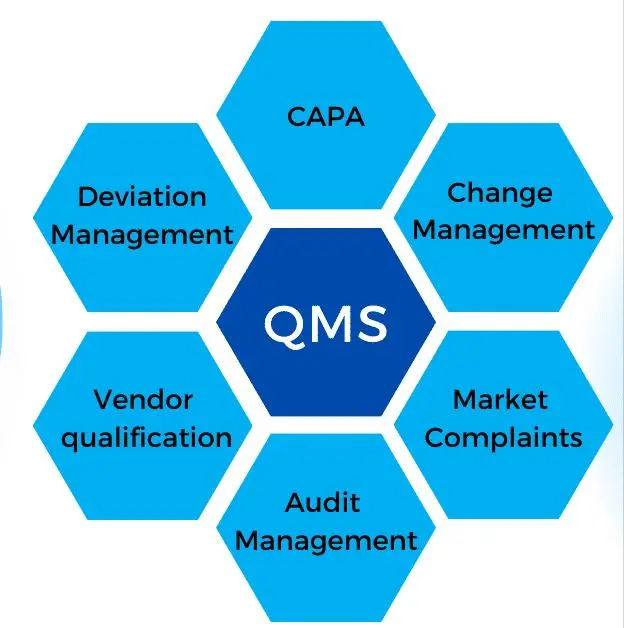
مفهوم سیستم کیفی دارویی در خطوط راهنماها
نگاهی عمیق به چارچوبهای بینالمللی برای تضمین کیفیت در صنعت داروسازی
در صنعت داروسازی، کیفیت تنها به معنای تطابق با مشخصات فیزیکی و شیمیایی نیست. کیفیت، مفهومی گسترده، پویا و سیستمی است که باید در تمامی مراحل چرخه عمر محصول—from development to distribution—بهصورت یکپارچه طراحی، پیادهسازی و پایش شود. این دیدگاه سیستمی در اسناد راهنمای کلیدی بینالمللی، با عنوان Pharmaceutical Quality System (PQS) یا سیستم کیفی دارو مورد تأکید قرار گرفته است.
⸻
تعریف سیستم کیفی دارو (PQS)
سیستم کیفی دارو مجموعهای از ساختارها، فرآیندها، سیاستها، منابع و فعالیتهایی است که برای تضمین مداوم کیفیت محصول دارویی طراحی شدهاند. این سیستم بر پایه اصول مدیریت کیفیت و الزامات مقرراتی بنا شده و هدف آن، ارائه محصولی ایمن، مؤثر و سازگار با انتظارات بیمار و الزامات رگولاتوری است.
⸻
منابع اصلی تعریف PQS
مفهوم سیستم کیفی دارو در چند سند کلیدی بینالمللی بهوضوح تشریح شده است:
•ICH Q10 – Pharmaceutical Quality System
•EU-GMP Part I Chapter 1 – Pharmaceutical Quality System
•WHO TRS 986 Annex 2
•PIC/S PE009 – GMP Guide
هر یک از این اسناد، با زبان و تمرکز خاص خود، بر اهمیت یک سیستم کیفی یکپارچه و پویا تأکید دارند.
⸻
عناصر کلیدی سیستم کیفی دارو
🔹 مدیریت دانش و مدیریت ریسک کیفی
مدیریت کیفیت دارو بدون تحلیل و مدیریت سیستماتیک ریسک ممکن نیست. استفاده از ابزارهای QRM به سازمانها کمک میکند تصمیماتی هوشمندانهتر و مستندتر بگیرند.
🔹 مدیریت تغییر (Change Management)
کنترل و ارزیابی علمی هرگونه تغییر در فرآیند، تجهیزات یا منابع انسانی بهمنظور پیشگیری از تأثیر منفی بر کیفیت.
🔹 انحرافات، اقدامات اصلاحی و پیشگیرانه (Deviation, CAPA)
شناسایی، تحلیل علل ریشهای و اصلاح فرآیندهای مشکلدار برای جلوگیری از تکرار آنها.
🔹 بررسی روندها و مرور کیفیت محصول (Trend Analysis, PQR)
پایش مستمر دادههای کیفی و تولیدی برای کشف الگوهای پنهان و جلوگیری از انحرافات آتی.
🔹 ممیزی داخلی و مدیریت تأمینکنندگان
ارزیابی مداوم عملکرد داخلی و کیفیت زنجیره تأمین برای حفظ یکپارچگی سیستم.
🔹 بازنگری مدیریت (Management Review)
ارزیابی دورهای عملکرد سیستم کیفی توسط مدیریت ارشد و اتخاذ تصمیمات بهبود.
⸻
هدف PQS فراتر از انطباق
سیستم کیفی دارو صرفاً برای پاسخگویی به بازرسان یا گذر از ممیزی طراحی نشده است. هدف PQS، ایجاد یک فرهنگ کیفیت است که در آن هر فرد، در هر سطح، خود را مسئول کیفیت میداند.
⸻
رویکرد AVISAN در طراحی و پیادهسازی PQS
ما در AVISAN با تکیه بر استانداردهای جهانی و تجربه اجرای موفق سیستمهای کیفیت در شرکتهای دارویی، خدمات زیر را در حوزه PQS ارائه میدهیم:
🔹 طراحی ساختار PQS بر اساس ICH Q10 و EU-GMP
🔹 آموزش تیمهای تخصصی در سطوح مختلف سازمان
🔹 اجرای پروژههای مستندسازی، ممیزی، ارزیابی شکاف و اصلاح ساختاری
🔹 استقرار ابزارهای مدیریت دانش و ریسک
🔹 ادغام سیستمهای کیفیت با فرآیندهای تولید، کنترل کیفیت و زنجیره تأمین
⸻
📌 یک سیستم کیفی واقعی، مستندسازی نیست؛ بلکه فرهنگسازی است. PQS ابزار شما برای ساختن سازمانی پایدار، پاسخگو و قابل اعتماد است.



دیدگاهتان را بنویسید